
Trong bài viết trước đây, tôi có đề cập việc phối hợp vaccine (trộn vaccine khác loại) chống Covid-19 (đọc TẠI ĐÂY). Tuy nhiên do tình hình dịch gia tăng, đang có nhiều bạn đọc tiếp tục đặt câu hỏi về việc này.
Câu hỏi càng trở nên cấp thiết hơn với việc Việt Nam đã chấp nhận sử dụng nhiều nguồn vaccine khác nhau trong việc chống Covid-19. Trong khi các vaccine đang được nhập về từ nhiều nguồn khác nhau với công nghệ chế tạo khác nhau, thì nguồn vaccine không phải lúc nào cũng đáp ứng được nhu cầu tiêm vaccine cho những người đã tiêm mũi đầu (prime, khởi động) bằng mũi thứ hai (boost, tăng cường) với cùng chủng loại.
Bài viết này nhằm nhắc lại vấn đề trộn vaccine, với giải thích cặn kẽ hơn về cơ sở lý thuyết miễn dịch học, và thực tế đang nghiên cứu áp dụng ở các quốc gia đã đi trước chúng ta trong việc chiến đấu với dịch bệnh. Mục tiêu là cung cấp thông tin để cơ quan chức năng cân nhắc các quy định về phối hợp vaccine, góp phần khắc phục khó khăn nói trên.
Kháng thể nhận biết họ hàng với nhau
Kháng thể là những phân tử miễn dịch quan trọng để bất hoạt mầm bệnh. Kháng thể do một loại tế bào miễn dịch có tên là lympho B và các tương bào (plasmocyte) tương ứng sản xuất ra. Khi cơ thể tiếp xúc với một phân tử protein lạ, hệ miễn dịch kích hoạt nhiều dòng tế bào lympho khác nhau nhận biết các bộ phận khác nhau của cùng một phân tử đó.
Mỗi bộ phận (hay đoạn chuỗi peptide) đặc hiệu cho một dòng tế bào lympho được gọi là một epitope (quyết định kháng nguyên). Do có nhiều dòng tế bào cùng nhận biết một phân tử, tập họp các kháng thể tạo ra được gọi là kháng thể đa dòng (polyclonal antibodies).
Khi các epitope ở gần nhau, hoặc xa nhau nhưng có cấu trúc tương tự, thì các dòng tế bào lympho tương ứng có khả năng nhận biết được epitope của nhau.
Các epitope kích hoạt lẫn nhau này gọi là cognate epitopes (epitope họ hàng), kháng thể gọi là cognate antibodies (kháng thể họ hàng). Việc kích hoạt miễn dịch bởi các epitope họ hàng tạo ra hiện tượng epitope spreading (lan tỏa quyết định kháng nguyên).
Ví dụ vi khuẩn hay virus thường chứa các phân tử bắt chước (mimic) các phân tử của chính cơ thể chúng ta, vì vậy sau khi bị bệnh nhiễm trùng, các tế bào lympho được kích hoạt chống lại mầm bệnh có thể lan tỏa quyết định kháng nguyên sang các phân tử của chính cơ thể, là nguyên nhân phát sinh các bệnh tự miễn.
Trong một ví dụ rất gần đây, các nhà khoa học đã thu thập các bằng chứng cho rằng biến chứng sinh huyết khối hiếm gặp nhưng rất nguy hiểm sau khi tiêm vaccine AstraZeneca chính là do hiện tượng lan tỏa quyết định kháng nguyên từ phức hợp chứa DNA của vaccine sang các phức hợp chứa heparin (chất chống đông máu). Công trình đã được đăng tải trên tờ Nature ra ngày 21/7/2021, tác giả đầu là Angela Huynh.
Một nhánh bảo vệ quan trọng khác chống Covid-19 là các tế bào lympho T gây độc, có khả năng tiêu hủy các tế bào nào đã bị nhiễm virus. Các vaccine gây ra được sự tổng hợp protein gai từ bên trong tế bào – ví dụ Pfizer hay AsstraZeneca, thì có nhiều khả năng kích ứng nhánh miễn dịch này.
Các vaccine Nanocovax hay Sinopharm chỉ đưa protein gai từ bên ngoài vào cơ thể, vì vậy ít có khả năng kích hoạt được lympho T gây độc. Tương tự như lympho B và kháng thể, lympho T cũng có các epitope họ hàng.
Protein Gai - Đích chung của đa số vaccine chống Covid-19
Phần lớn, nếu không nói là tất cả các vaccine chống Covid-19 hiện nay đều vào nhằm mục tiêu là phân tử protein gai (protein S nằm trên bề mặt virus, là "cánh tay" để virus bám vào được màng tế bào và lọt được vào bên trong).
Vaccine Pfizer hay Moderna dùng đoạn mRNA mã hóa ra protein gai, đưa vào cơ thể bằng những nang lipid cực nhỏ, các nang này khi được tế bào nuốt vào thì mRNA điều khiển tổng hợp ra protein gai.
Vaccine AstraZeneca và Sputnik 5 thì nạp đoạn gene (DNA) mã hóa protein gai vào virus lành tính, khi virus này được tiêm vào cơ thể thì DNA tổng hợp ra mRNA, rồi mRNA điều khiển tổng hợp ra protein gai.
Vaccine Sinopharm và Sinovac sử dụng nguyên cả virus SARS-CoV-2 đã bất hoạt, trong đó có chứa protein gai.
Vaccine Nanocovax do Việt Nam đang thử nghiệm lâm sàng giai đoạn 3 thì sử dụng protein gai tinh khiết.
Tất cả đều có tác dụng kích hoạt tạo ra các kháng thể đa dòng nhận biết protein gai của Covid-19.
Trong số các kháng thể đa dòng này sẽ có một số đơn dòng họ hàng nhận biết được bộ phận protein gai trực tiếp tương tác với màng tế bào. Hiệu quả bảo vệ của vaccine phụ thuộc chủ yếu vào nhóm các đơn dòng này và khả năng chúng có thể lan tỏa quyết định kháng nguyên cho nhau.
Kết hợp Vaccine - chiến lược đã có từ lâu nhưng vẫn cần được nghiên cứu thêm
Việc kết hợp vaccine có cơ sở lý thuyết miễn dịch học và tiềm năng lợi ích thực tế, vì vậy đã được các nhà khoa học nghiên cứu từ lâu với các mầm bệnh như cúm mùa, HIV, Ebola.
Trong ví dụ vaccine chống virus Ebola, người ta nạp gene (đoạn DNA) mã hóa protein bề mặt của virus Ebola vào một virus lành tính tên là adenovirus, tạm gọi là virus A, và dùng virus A làm vaccine. Khi tiêm virus A vào cơ thể, protein bề mặt được tổng hợp ra sẽ kích hoạt hệ miễn dịch tạo ra kháng thể kháng protein bề mặt trung hòa được virus.
Nhưng khi tiêm mũi vaccine tăng cường cùng chủng loại virus A, hệ miễn dịch bị kích hoạt mạnh với toàn bộ hạt virus A thay vì phải tập trung vào protein bề mặt. Kết quả là đáp ứng miễn dịch với riêng protein bề mặt có thể bị pha loãng đi, thay vì cần phải được tăng cường.
Để tránh được hiện tượng nói trên, viện Gamaleya (Nga) đã nghiên cứu thay virus A (adenovirus) bằng một virus lành tính khác (vesicular stomatitis virus), tạm gọi là virus B cũng được nạp gene protein gai, và dùng virus B này làm vaccine tăng cường để chống Ebola (1).
Tương tự như vậy, vaccine chống Ebola do Johnson & Johnson chế tạo (dùng adenovirus) cũng đã được nghiên cứu phối hợp với vaccine dùng virus khác loài (1).
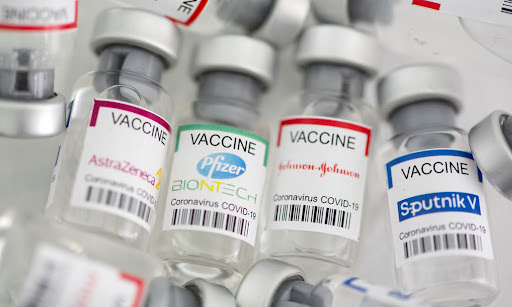
Từ kinh nghiệm nói trên có thể suy ra trong trường hợp vaccine chống Covid-19 bằng các công nghệ như của AstraZeneca (dùng adenovirus) hay Sinopharm hay Sinovac (dùng toàn hạt nCoV đã bất hoạt), việc dùng một vaccine khác chủng loại sẽ có khả năng tập trung tăng cường các kháng thể đặc hiệu với protein gai thay vì các kháng thể với các bộ phận khác của virus vốn không có tác dụng trung hòa.
Tuy nhiên trong y học, mỗi khi chúng ta dùng một thuốc mới hay một phác đồ mới thì đều phải có thử nghiệm lâm sàng chứng minh là an toàn và có hiệu quả.
Thêm nữa, nghiên cứu kết hợp vaccine sẽ góp phần quan trọng giải quyết các khó khăn về hậu cần, khi không phải lúc nào cũng có sẵn vaccine cùng chủng loại để tiêm mũi tăng cường.
Vì vậy, các quốc gia có tiềm lực cao về công nghệ vaccine đang tích cực đi đầu trong các nghiên cứu phối hợp vaccine.
Trộn vaccine Covid-19: Các kết quả từ các nước đi trước
Tuy các vaccine AstraZeneca của ĐH Oxford (Anh) và Sputnik 5 của Viện Gamaleya (Nga) có cùng nguyên lý là vaccine DNA, nhưng lại sử dụng các virus mang vector khác nhau. Trên cơ sở đó hai bên đã hợp tác thực hiện 2 cuộc thử nghiệm lâm sàng trộn 2 loại vaccine này, một tại Nga và một tại Azerbaijan. Kết quả đang chờ bộ Y tế Nga chấp thuận (2).
Tại China, sau các thông báo về hiệu quả tương đối thấp của các vaccine toàn hạt (Sinopharm và Sinovac), Cơ quan Quản lý Dược của nước này (China’s National Institutes for Food and Drug Control) đang tiến hành thử nghiệm kết hợp 4 loại vaccine dựa trên các công nghệ hoàn toàn khác nhau: vaccine toàn hạt, vaccine protein tái tổ hợp, vaccine DNA và vaccine RNA (2).
Một thử nghiệm lâm sàng của ĐH Oxford có tên là Com.Cov kết hợp 2 loại vaccine có công nghệ hoàn toàn khác nhau, là AstraZeneca (vaccine DNA với virus vector, sau đây viết tắt là DNA) và Pfizer (vaccine mRNA, sau đây viết tắt là RNA) vừa được công bố trên tờ Lancet số ra 4/9/2021. Thử nghiệm này bao gồm 830 tình nguyện viên trên 50 tuổi, được chia làm 4 nhóm.
Kết quả 4 nhóm (mũi 1/mũi 2) được xếp hạng theo hiệu giá kháng thể kháng protein gai như sau: DNA/DNA (14080), DNA/RNA (12906), RNA/DNA (7133), và DNA/DNA (1392). Có thể ngoại suy ra lợi ích lớn nhất là cho người đã tiêm mũi 1 là AstraZeneca và mũi 2 là Pfizer. Quan trọng nhất, có 4 trường hợp biến chứng nặng, phân bố đều 1 trường hợp cho mỗi nhóm, nhưng đều được kết luận không liên quan đến quy trình vaccine (3).
Các thử nghiệm lâm sàng tương tự cũng được tiến hành tại Tây Ban Nha, Đức và Pháp (4).
Vì các thử nghiệm lâm sàng này có số lượng mẫu còn nhỏ, WHO cho đến ngày 12/6/2021 vẫn cho rằng các nước cần phải thận trọng với chiến lược này (5).
Tuy nhiên, theo một điều tra do Reuters công bố 16/8/2021, khá nhiều quốc gia như Campuchia, Đan Mạch, Đức, Indonesia, Nga, Thổ Nhĩ Kỳ, Anh Quốc và Hoa Kỳ đang chọn sách lược này để đối phó với các khó khăn về nguồn cung cấp vaccine, hoặc do các hạn chế trong việc dùng vaccine cùng chủng loại (5).
Tại Đức, trong khi dân chúng còn nhiều lo ngại về chiến lược trộn vaccine, bà thủ tướng Angela Merkel trước đó đã được tiêm mũi 1 bằng AstraZeneca đã làm gương với việc tiêm mũi 2 bằng vaccine Moderna có nguyên lý chế tạo hoàn toàn khác (BBC News, 22/7/2021).
Tham khảo:
1- https://ec.europa.eu/research-and-innovation/en/horizon-magazine/five-things-know-about-mixing-and-matching-coronavirus-vaccines
2- https://www.nytimes.com/2021/03/30/health/coronavirus-vaccine-astrazeneca-pfizer.html
3- https://www.nature.com/articles/d41586-021-01805-2
4- https://www.reuters.com/business/healthcare-pharmaceuticals/spain-trial-mixing-covid-vaccines-after-restricting-astrazeneca-shot-2021-04-19/
5- https://www.reuters.com/world/middle-east/countries-weigh-mix-match-covid-19-vaccines-2021-05-24/